血液内科の主な疾患と
治療方法
急性骨髄性白血病
主な症状
貧血、感染、出血傾向
解説
急性骨髄性白血病(AML)を含め、血液のがんの分類は主にがん細胞の形態をもとにして1976年にFAB分類が提唱されました。AMLではM0からM7まで8種類に分類されましたが、白血病の原因となる遺伝子とそのメカニズムが明らかにされるにつれ、現在ではWHOの分類が一般的です。FAB分類とWHO分類の違いは、後者は原因となる遺伝子や染色体異常を加味したことで、骨髄中の芽球(もっとも幼若な細胞)比率も「30%以上」から「20%以上」へと引き下げられています。
血液を作る場所である骨髄にがん細胞が増えると正常の血液細胞が産生されなくなります。正常の白血球の数が減ると感染を起こしやすくなり、また打撲した覚えがないのに紫色のあざができたり、鼻血や歯茎からの出血で異常に気がつくこともあります。感染症も出血も場合によっては死亡につながりますので、入院治療が必要です。
治療方法
一般的に、活動性の感染症がなく、心臓や腎臓などの重要臓器の機能が低下していない場合には複数の抗がん剤を組み合わせた治療が基本となります。抗がん剤を投与することで体内の白血病細胞を1 / 10000以下に減らすことができれば、末梢血や骨髄から白血病細胞がなくなったように見え、この状態を「寛解」と呼びます。発病時に白血病細胞は1012個程度ありますので、「寛解」とはいえ、まだまだ体内には白血病細胞が残っています。そのために寛解後にも地固め療法や強化療法など、複数回の治療が必要となります。最も強い地固め療法の一つが造血幹細胞移植です。
急性前骨髄性白血病はビタミンAの誘導体であるレチノイン酸が非常によく効く白血病で、多種類の抗がん剤を組み合わせた治療の前にレチノイン酸の経口内服を行います。
寛解を得るために行う治療を寛解導入療法と呼びますが、基礎疾患に加えて抗がん剤治療による正常細胞の減少のために感染や出血が起こりやすく、これらの合併症を予防する治療を併用します。
再発すると従来の抗がん剤治療では長期間の生命予後は期待できないので、造血幹細胞移植が考慮されます。使用する幹細胞の種類や移植のための治療(前処置と言います)の異なる移植治療があります。詳しくは用語集の造血幹細胞移植の欄を御参照下さい。
骨髄異形成症候群
主な症状
貧血、感染、出血傾向。症状がなく偶然見つかることもあります。
解説
骨髄異形性症候群(MDSと言われます)は骨髄の細胞が異形性、つまり異常な形をもつようになった病気の集まりを示し、病気が進行すると急性骨髄性白血病に移行することもある、血液がんの一種です。
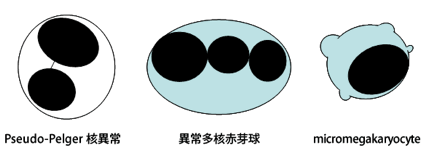
世界保健機構(WHO)ではMDSを以下の8種類の病型に分類しています。
- 一系統の不応性血球減少(RA,RN,RT)
- 鉄芽球性貧血(RARS; 15%≦環状鉄芽球)
- 多系統の異形性を伴う不応性血球減少(RCMD)
- 多系統の異形性を伴う鉄芽球性貧血(RCMD-RS)
- 芽球増加を伴う不応性貧血(RAEB-1; 5≦骨髄中芽球<10%)
- 芽球増加を伴う不応性貧血(RAEB-2; 10≦骨髄中芽球<20%)
- 分類不能型MDS(異形性は10%未満だがMDSに特徴的な染色体異常がある)
- 5q-染色体異常をもつMDS
MDSの生命予後判定のためにIPSSと呼ばれる国際スコアがあります。血球減少の程度、骨髄中の芽球の数、染色体異常を点数化して判断し、治療方針を立てます。2012年秋には新しくIPSS-Rという予後予測システムが提唱されました。今後この新しいシステムを使用して治療方針決定が行われるものと考えられます。
治療方法
年齢やMDSのタイプにより選択する治療法が異なります
経過観察
血球減少が著明でなく、芽球増加も著しくない場合に選択されます。
輸血、造血刺激因子などの支持療法
貧血や易出血傾向に対する輸血療法や感染の治療を行います。頻回の輸血が原因で鉄が種々の臓器に蓄積すると色々な障害が引き起こされるので、鉄過剰症に対して除鉄療法を行う場合もあります。
抗がん剤療法
芽球が増えるタイプのMDSの治療に用いられます。複数回の治療を必要とします。最近はDNAの低メチル化促進剤が頻用されるようになっています。
免疫抑制剤
予後不良染色体異常がないある種のMDSで用いられます。
ビタミン療法(ビタミンKやビタミンD)
稀に効果を示すことが報告されています。
造血幹細胞移植
MDSに対し治癒が望める唯一の治療法ですが、体に対する負担が大きいため非高齢者のみが適応となります。MDSは高齢者に多い疾患で、通常の移植は成績が悪かったのですが、移植前処置を工夫して高齢者の患者様にも同種造血幹細胞移植を実施する試みがなされています。移植が可能かどうかは主治医の先生から説明を受けてください。
次世代の治療
これまでの薬剤とは作用機序が異なる、新しい治療薬が開発されてきています。欧米に遅れてわが国でも2011年3月アザシチヂンという薬が認可され臨床使用が可能となりました。また5q-の核型異常を持つMDSにはレナリドマイドという薬が奏功することが知られており、日本でも2010年から使用できるようになっています。
慢性骨髄性白血病
主な症状
全身倦怠感、脾腫、関節痛、発熱など。
解説
慢性骨髄性白血病の幹細胞では9番目の染色体にあるbcr遺伝子と22番目の染色体上にあるabl遺伝子が染色体転座で融合して、新たにbcr/abl 遺伝子ができます。この遺伝子から作られたBCR/ABL蛋白は細胞の増殖のスイッチを入りっぱなしにしますので、白血球や血小板がどんどん増えてしまうわけです。
以前は抗がん剤を使用して白血球の数をコントロールできても、治癒させることはできませんでした。そのため同種造血幹細胞のみが完治を期待しうる治療法でしたが、治療に伴う合併症の頻度も高く、全ての患者さんに移植治療ができるわけではありません。
最近染色体転座で新たにできた異常遺伝子の産物であるBCR/ABL蛋白を特異的に阻害する薬剤(分子標的薬)が開発されました。この薬を内服することで大きな副作用なく、ほとんどの患者さんが長期間にわたりいい状態で過ごすことができるようになっています。病気についての詳しい説明は用語集の慢性骨髄性白血病の項を御参照下さい。
治療方法
分子標的治療薬であるグリベックが使用できるまでは、インターフェロンと造血幹細胞移植以外には治癒の可能性はありませんでした。欧米を中心にしたグリベックの臨床試験により、現在では最初に行うべき治療としてグリベックが推奨されています。
- チロシンキナーゼ阻害剤
9番染色体上のbcr遺伝子と22番染色体上のabl遺伝子が融合したbcr/abl遺伝子からは通常にはないBCR/ABL蛋白が作られ、細胞の増殖スイッチを恒常的にonの状態にしています。グリベックなどのチロシンキナーゼ阻害剤はこの蛋白が働くときに必要なエネルギー源であるATPが結合できなくなるように設計されたお薬です。現在日本国内で使用可能なチロシンキナーゼには3種類あり(グリベック、タシグナ、スプリセル)、副作用はそれぞれ異なりますが、むくみ、筋肉痛、皮疹、下痢、肝機能障害、膵炎などがあり、主治医の先生から十分な説明を受けてください。またこの薬の治療が予定通り順調に効果が出ているかどうかを判断するために定期的に血液検査や骨髄検査が必要で、決められた時間までに目標を達成できないときには、他の治療法が考慮されることになります。 - インターフェロン
グリベックが使用可能となるまでは移植以外の治療法としてよく使用されていました。正確な効果発現の機序は分かっていませんが、インターフェロンを使い続けることで、腫瘍細胞が減少、あるいは消失することが報告されています。キロサイドという薬と併用するほうがより効果的といわれています。何らかの理由で分子標的治療や移植治療ができない患者さんには試みるべき治療です。 - 抗がん剤
病気を治す力はありませんが、白血球数をコントロールするために現在でも時に使用されています。ハイドロキシウレアが一般的ですが、頻度は低いものの(1%以下)、長期投与で皮膚潰瘍(特に下肢に好発)を発症することがあると報告されています。 - 造血幹細胞移植
チロシンキナーゼ阻害剤が抵抗性となった場合には同種造血幹細胞移植のみが治癒の可能性を持った治療法です。同種造血幹細胞移植はドナーさんのリンパ球の力を借りて白血病細胞を殺そうとするものです。造血幹細胞移植の詳しい説明は用語集の造血幹細胞移植の項を御参照下さい。
慢性骨髄増殖性疾患
主な症状
血栓、塞栓。疾患の後期には骨髄線維症に伴う血球減少による症状。
解説
骨髄での造血が異常に亢進し、多くの場合は血球が増加します。増える細胞の種類により、真性多血症、特発性血小板血症、骨髄線維症に分類されますが、患者さんの生活の質を決定する点で重要なものに、血管の閉塞があります。動脈、静脈共に閉塞しやすくなり、特に心臓の血管で閉塞が起こると心筋梗塞につながりますので、現時点での治療の目的はこれら血管病変の予防に重点が置かれています。骨髄線維症は真性多血症や特発性血小板血症の進行期にも起こり、骨髄での造血が著しく損なわれ、血球減少をきたします。この場合には白血病などと同様に、感染や出血が起こりやすくなります。
骨髄増殖性疾患はそれ自体はがんではありません。しかしながら、一部の患者さんは急性白血病を発症することが知られています。遺伝子異常がさらに加わることで細胞のがん化が起こってくると考えられますが、どの遺伝子が、どのような原因で白血病を起こしてくるのかは不明で、多くの研究者によって解明の努力が続けられています。
もう少し詳しくお知りになりたい方は、用語集の骨髄増殖性疾患の項を御参照下さい。
治療方法
血栓、塞栓の予防
血栓の危険因子は当初血小板数と考えられ、60万 / μL以下に減らすことを目標として、薬物治療された時期がありました。しかしながら、多くの患者さんを対象とした研究からは、血小板数と血栓の危険性は相関せず、年齢が60歳以上であること、過去に血管の閉塞をきたしたことがあること、さらに最近分ったことですが、白血球数が多いこと、が血栓の危険因子であるとされています。真性多血症では赤血球数を下げるために瀉血療法は全ての患者さんに実施され、ヘマトクリットの値を45%以下に維持することが推奨されています。さらに、特に禁忌でない限り全ての患者さんに血小板凝集抑制剤であるアスピリンの投与が勧められています。危険因子を持っていらっしゃる患者さんでは上記に加えて化学療法(ハイドロキシウレア)が実施されます。一般に化学療法は発癌作用を持つことが多く、その投与にはメリットとデメリットの比較のうえに投与されるべきとされますが、ハイドロキシウレアは最も発癌作用の少ないものとして、多く使用されています。他の薬剤としてインターフェロンαも有効とされていますが、治療費の観点からは他の方法が効果がないときに考慮されます。
分子標的薬
骨髄増殖性疾患の仲間である慢性骨髄性白血病では、その原因遺伝子が解明され、異常遺伝子産物を選択的に阻害する薬剤、分子標的療法剤が臨床応用され、劇的な効果があることが分っています。標的となる遺伝子産物が異なりますが、最近アメリカではJAK2に対する選択的な阻害薬が開発され、臨床試験で有効であることが専門雑誌で報告されました。まだ日本では使用できませんが、そう遠くない未来に新しい治療法が導入されることが期待されます。
骨髄線維症へと進展した場合には、最終的には血液細胞を充分に造ることができなくなり、貧血、白血球減少、血小板減少をきたします。残念ながら骨髄線維症に対する有効な治療法はなく、若年者では造血幹細胞移植のみが根治療法です。
急性リンパ性白血病
主な症状
貧血症状、易感染性、出血傾向
解説
血液のがんは悪性化した細胞の特徴で骨髄性、リンパ性などに、またがん細胞の増える速度により急性と慢性に分類されています。血液の幹細胞(すべての血液細胞の大元になる未熟な細胞)からは、主に赤血球、顆粒球、血小板へと分化する骨髄性の幹細胞と、リンパ節でT、Bリンパ球へと分化するリンパ系の幹細胞とに別れると信じられています。リンパ系の細胞になるべき幹細胞で異常が起こってがん細胞になり、かつ、がん細胞が急激に増えるタイプの白血病を急性リンパ性白血病と呼びます。
子供に高率に発生するタイプが知られていますが、一般的に大人の急性リンパ性白血病に比べ、抗がん剤がよく効きます。大人で発症した急性リンパ性白血病は、急性骨髄性白血病と比べ、抗がん剤治療の成績が少し低いといわれています。白血病細胞は血液の中だけではなく、肝臓、脾臓などにも浸潤しますし、またしばしば中枢神経(脳や脊髄神経)へ浸潤することもあります。
がん化する原因はよく分かっていませんが、特徴的な染色体異常を持つタイプがあり、近年がん遺伝子の研究が精力的に進められています。慢性骨髄性白血病と同じ9番と22番の染色体が相互転座を起こし、Ph1染色体を有する急性リンパ性白血病は大人の急性リンパ性白血病の約25%を占め、治療抵抗性であることが多いと言われています。
治療方法
抗がん剤による化学療法と造血幹細胞移植が主体です。成人発症の急性リンパ性白血病は抗がん剤投与で寛解状態(がん細胞が当初の1 / 10000)となっても、その後に再発する危険性が高く、可能な場合には同種造血幹細胞移植を実施することが推奨されています。
Ph1染色体陽性の急性リンパ性白血病は治療抵抗性のことが多く、治療に難渋していたのですが、分子標的治療薬の併用により成績の向上が期待できるようになっています。寛解後の最も強い地固め療法である同種造血幹細胞移植については用語集の中の造血幹細胞移植の項を御参照下さい。
慢性リンパ性白血病
主な症状
リンパ節腫大、肝脾腫、貧血、全身倦怠感
解説
成熟したリンパ球様の細胞が骨髄と末梢血で増える病気で、高齢者に多く発症します。増えてくるリンパ球の種類によってB細胞性とT細胞性に分けられますが、前者の方が圧倒的に頻度が高く、一般的に慢性リンパ性白血病といえばB細胞型を指すことが多いようです。欧米など白色人種では頻度の高い病気ですが、日本人では2~3%と欧米に比べ発症率は1 / 10といわれます。
治療方法
病気の進行は緩徐で、初期にはほとんど症状がありません。また、他の造血器腫瘍と異なり根治を目指す有効な治療法がないことから、ある程度進行するまでは治療を実施しない、"watch and wait"が基本的な方針とされています。貧血や脾腫の出現など、病期が進行した場合にはアルキル化剤やプリン拮抗薬が単独もしくは組み合わせで使用されます。代表的なお薬としては、シクロフォスファミド(エンドキサン®)、フルダラビン(フルダラ®)、リツキシマブ(リツキサン®)などがあります。最近抗CD20抗体のオファツムマブ(アーゼラ®)がわが国で慢性リンパ性白血病への保険適応が認められ、臨床使用できるようになりました。造血器腫瘍に対する根治療法としての同種造血幹細胞移植は現時点ではまだ研究的な治療としての位置づけで、若年者でかつ治療抵抗性の場合に限って試みられています。
日常生活での注意点としては、抵抗力が低下しますので、感染予防が重要です。免疫グロブリンが低下し頻回に感染症を起こす場合には、IgGが400mg / dl以上となるように補充療法を行うことがあります。
悪性リンパ腫
主な症状
リンパ節腫大、肝脾腫大、発熱
解説
リンパ球は体内に侵入してきた異物(ウイルスや細菌など)を除去する役割を持った、免疫の要になる細胞で、私達の体を異物から守ってくれています。リンパ球の中にはB細胞、T細胞、NK細胞といった種類があり、骨の中にある「骨髄」という組織でつくられ、頭から足の先まで行き届いているリンパ管や血管を通って、全身に分布します。リンパ球ががん化すると、無制限に増殖する上に、体内に侵入してきた異物を除去するという正常な機能を果たさなくなります。主には
- 無制限に増殖する⇒リンパ節が腫れる(首や腋の下、足の付け根などにしこり=腫れたリンパ節ができます。多くの場合、痛みはありません。)
- 原因不明の熱(微熱のこともあれば、38℃以上の熱のこともあります。)
- 6ヶ月の間に体重が10%以上減少する
- 体がだるい
- 寝汗をかく
- 免疫力の低下、感染症を起こしやすい
といった症状が出現します。
リンパ腫の原因となった細胞の種類、増殖の速さなどにより治療方針が異なるので、正確な診断がとても重要です。腫れたリンパ節を生検したり、病変の広がりを明らかにするため骨髄検査、エコー検査やCT検査を実施します。
多発性骨髄腫
主な症状
貧血、易感染性、出血傾向、骨痛、骨折、腎不全
解説
多発性骨髄腫は、血液細胞のひとつである「形質細胞」ががん化した、血液の悪性疾患です。形質細胞はBリンパ球が成熟した細胞で、免疫グロブリン(抗体)という病原菌から体を守る働きをするタンパク質をつくっています。がん化した異常形質細胞から産生される異常な免疫グロブリンはM蛋白と呼ばれ、感染防御の働きをしません。正常では形質細胞は骨髄に1%未満の割合でしか存在しませんが、多発性骨髄腫では10%以上に増加し、正常の血液細胞が造られるのを阻害します。また骨の破壊をきたし、カルシウムが溶け出すことによって血液中のカルシウムが高くなります(高カルシウム血症)。従って、多発性骨髄腫では他の血液の悪性疾患と同じように正常の血液が作られなくなると同時に、異常蛋白が血液中で増加し腎臓の機能を低下させ、また骨が溶けることで骨折の原因となったり、高カルシウム血症のための意識障害や急性腎不全など、多彩な症状が出現します。
種々の新しい抗腫瘍剤が開発され血液癌の一部は治癒するようになりましたが、骨髄種に対しては長い間有効な治療法が無く、生存期間は余り改善しませんでした。しかしこの数年、多くの新規の薬剤が開発され大幅に治療成績が向上しています。新規薬剤と造血幹細胞移植を組み合わせることで、多発性骨髄腫も治癒する病気の仲間入りをするかもしれません。
治療方法
多発性骨髄腫の治療は大きく次の6つに分かれます。
- 治療せずに観察していく
病勢がゆっくりで臓器障害がなく、骨病変がない場合選択されます。 - MP療法+ビスフォスフォネート製剤
以前より行われてきた標準的治療法で抗がん剤とステロイド剤を4日間内服します。骨折予防にビスフォスフォネート製剤の点滴を併用します。 - 自己末梢血幹細胞移植
非高齢者の方を対象に施行される治療法です。抗がん剤治療を何回か施行した後、自己の造血幹細胞を血球分離装置を用いて採取します。その後、造血幹細胞で造血をサポートしながら大量の抗がん剤を投与して骨髄腫細胞にダメージを与えるという方法です。 - 新規薬剤
サリドマイド、レナリドマイドやボルテゾミブといった骨髄腫に対する新しい薬剤が認可され骨髄腫の治療は格段に進歩しました。ただし特徴的な副作用があるので注意が必要です。 - 放射線療法
腫瘤を形成した部位や痛みの強い場所に施行します。抗がん剤治療とよく併用されます。 - 同種造血幹細胞移植
非高齢者の方を対象に施行される治療法です。この病気に対しては、まだこれからの治療ですので詳細は主治医に確認してください。
用語集の中の多発性骨髄腫の項も御参照下さい。
再生不良性貧血
主な症状
貧血、感染、出血傾向
解説
造血工場である骨髄内の血液幹細胞の障害によって全ての血球が減少する疾患です。汎血球減少をきたすほかの病気が否定されることが必要です。大きくは先天性(Fanconi貧血)と後天性に分かれますが、内科領域では後者が大半を占めます。後天性再生不良性貧血はさらに原因不明の特発性と、薬剤・放射線・ウイルスなどが原因で起こる二次性に分けられます。
治療方法
軽症、中等症の貧血の治療には蛋白同化ホルモンが主体となりますが、重症型では移植可能年齢の患者さんには造血幹細胞移植が選択されます。特発性のタイプの中には一部免疫が関与しているものがあり、シクロスポリンや抗ヒトTリンパ球抗体などの免疫抑制剤が使用されることがあります。
特発性血小板減少性紫斑病
主な症状
出血傾向
解説
原因不明という観点から「特発性」血小板減少性紫斑病とされますが、血小板破壊の機序は自己抗体によることが大半で、「免疫性」血小板減少性紫斑病とも呼ばれます。血小板の破壊には補体を介した直接の破壊亢進以外に、自己抗体が結合した血小板を網内系のマクロファージが貪食する機序もあります。SLEなどの自己免疫疾患との合併も多く認められ、若い女性で血小板が減少しているときは膠原病の検査も必要です。
治療方法
治療にはステロイドを含めた免疫抑制剤の投与や摘脾に加え、大量の免疫グロブリン投与が有効なことが多いとされます。これらはいずれも血小板の破壊を改善させることで血小板数の増加を期待するものですが、最近骨髄中の巨核球(血小板を産生している細胞)を直接刺激し、より多く産生させることにより血小板数を増加させる薬剤が使用可能となりました。これにより、ステロイドの副作用の軽減が期待できます。
-
- 循環器内科の主な疾患と治療方法
- 内分泌代謝・ダイアベティス(糖尿病)センターの主な疾患と治療方法
- 消化器・肝胆膵内科の主な疾患と治療方法
- 消化器外科の主な疾患と治療方法
- 血液内科の主な疾患と治療方法
- リウマチ・膠原病内科の主な疾患と治療方法
- 腫瘍内科の主な疾患と治療方法
- 脳神経内科の主な疾患と治療方法
- 乳腺外科の主な疾患と治療方法
- 整形外科の主な疾患と治療方法
- リハビリテーション科の主な疾患と治療方法
- 呼吸器外科の主な疾患と治療方法
- 形成再建外科の主な疾患と治療方法
- 皮膚科の主な疾患と治療方法
- 泌尿器科の主な疾患と治療方法
- 婦人科の主な疾患と治療方法
- 眼科の主な疾患と治療方法
- 耳鼻咽喉科の主な疾患と治療方法


